Departamento Editorial de Grupo Franja
El virus del herpes simple, específicamente el tipo 1 (HSV-1), es un virus ADN de doble cadena lineal que, al infectar la córnea, es capaz de desencadenar una marcada respuesta inmune, generando lesiones que podrían llevar a la discapacidad visual. Entre los daños registrados por este patógeno se encuentran: opacidad corneal, edema que puede ser severo, cicatrización y neovascularización, todos ellos motivo de especial preocupación.
Como se conoce, la infección por HSV en la córnea presenta un amplio espectro de reacciones del tejido, desde la afectación del epitelio y sus patrones dendríticos característicos hasta los daños en el estroma y las capas profundas adyacentes. Este artículo se enfocará en la queratitis estromal por HSV.
En la patogénesis de la queratitis estromal por herpes simple (KHS), es necesario comenzar identificando el proceso de replicación del virus desde las células epiteliales. Para desencadenar la respuesta del sistema inmune, es fundamental comenzar con el reconocimiento inicial del virus por parte de los receptores tipo Toll (TLRs) en la superficie celular, lo que estimula una cascada de respuestas intracelulares. Estos receptores son conocidos por ser tipo PRR (receptores de conocimiento de patrones), especializados en identificar patrones moleculares de antígenos que pueden ser patógenos o derivados de lesiones.
Una vez que el TLR actúa, se desencadena una vía de señalización importante, como es la de TRIF (TIR-domain-containing adapter-inducing interferon-β). Este adaptador que contiene el Dominio TIR que Induce Interferón-β, es una proteína que induce la producción de interferones de tipo I, que son moléculas clave en la respuesta antiviral del sistema inmunológico.
Otra molécula importante en la vía de los TLR es TRAF6 (TNF receptor-associated factor 6). Este receptor del factor de necrosis tumoral asociado al factor 6 es otra proteína adaptadora que participa en la señalización celular y está involucrada en las respuestas inmunitarias innatas y adaptativas. TRAF6 juega un papel destacado en la vía de señalización del receptor del factor de necrosis tumoral (TNF) y también se implica en la señalización de los receptores tipo Toll y otros receptores involucrados en el reconocimiento de patógenos. La activación de TRAF6 desencadena la producción de moléculas señalizadoras como el factor nuclear kappa B (NF-κB) y las quinasas relacionadas con la interleucina-1 (IL-1). Estas moléculas son esenciales para la regulación de las respuestas inflamatorias y las respuestas inmunitarias.
En relación con el factor (NF-κB), su función radica especialmente como factor de transcripción, es decir, una proteína que regula la expresión de genes al unirse a regiones específicas del ADN. Esta transcripción incluye la expresión génica que codifica para producir citoquinas como el TNF y las interleuquinas (IL), así como la producción de moléculas de adhesión que son esenciales para la comunicación entre células inmunitarias.
En cuanto a MYD88, esta es una proteína adaptadora en la señalización inmunitaria, mientras que PI3K-Akt es una vía de señalización celular que desempeña un papel clave en la regulación de procesos celulares fundamentales. Ambos son componentes importantes de la respuesta inmunitaria, de la regulación del crecimiento y la supervivencia celulares.
Toda la producción de células inflamatorias, citoquinas y quimioquinas es responsable de la infiltración gradual en el estroma. Estos componentes inflamatorios incluyen neutrófilos, células dendríticas (CD), células asesinas naturales (NK), que limitan la replicación viral mediante la producción de interferones de tipo 1 (IFNs) a partir de las células epiteliales corneales. Esto resulta en una actividad antiviral mejorada. Además, participan los macrófagos, capaces de fagocitar partículas virales y células infectadas. Aunque esta respuesta parece infalible contra los virus, se conoce el efecto destructivo que estos pueden generar a nivel intracelular.
A nivel exterior, cuando el complejo mayor de histocompatibilidad II (MHC-II) transmite la información presentada por las células presentadoras de antígeno (APCs) a la superficie de las células T helper (Th), se estimula la inducción de citocinas y quimioquinas, desencadenando eventualmente respuestas inmunitarias adaptativas que son una forma de hipersensibilidad de tipo retardado. Las células Th1 y Th17 son dos categorías de células T CD4+, que desempeñan un papel importante en la mediación de la respuesta inmunitaria inflamatoria de la queratitis herpética simple (HSK). También es relevante destacar que la combinación de la sustancia P (SP), un neuropéptido presente en la superficie ocular, y el receptor de neuroquinina-1 (NK1R), constituyen una vía que activa el factor nuclear (NF-κB), aumentando así los niveles de citocinas inflamatorias y quimiocinas. Con esto, se evidencia que la respuesta inmune al HSV es compleja, y que, dependiendo de la cantidad de mediadores inflamatorios y de la respuesta celular, se determina la severidad del daño estromal y el pronóstico visual. Ver Figura 1.
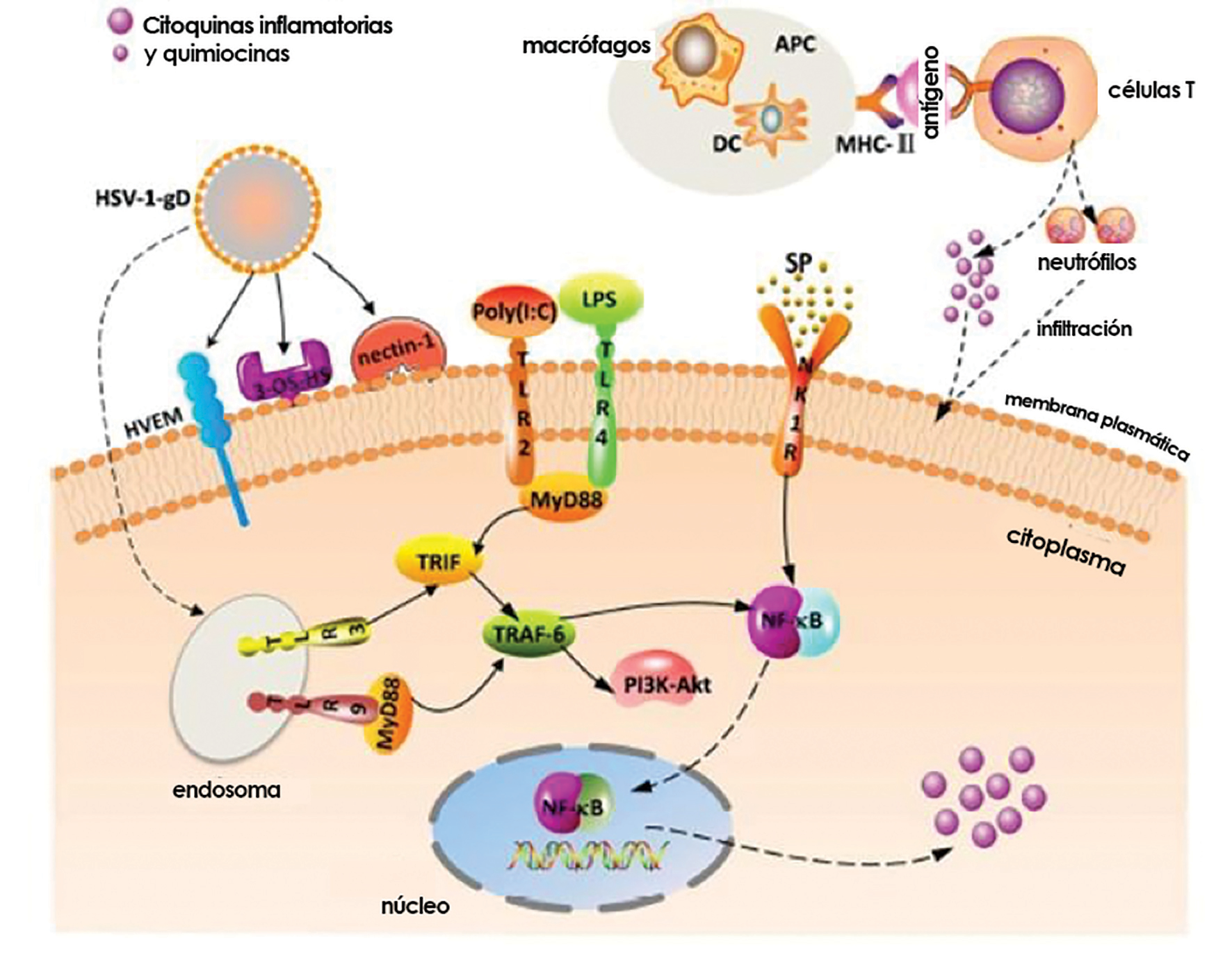
Adaptado de:
1. Wang L, Wang R, Xu C, Zhou H. Pathogenesis of Herpes Stromal Keratitis: Immune Inflammatory Response Mediated by Inflammatory Regulators. Vol. 11, Frontiers in Immunology. Frontiers Media S.A.; 2020.
.
.






