El ojo seco, una de las principales causas de consulta en la atención de la salud visual. En los últimos años, el aumento de su prevalencia ha planteado nuevos retos en cuanto a las estrategias terapéuticas a implementar. (1) La publicación de 2023 del TFOS sobre el impacto del estilo de vida en la superficie ocular destaca que esta condición tiene múltiples etiologías. (2) Además, subraya que el ojo seco es una entidad fisiopatológica compleja, lo que implica que el tratamiento debe ser integral y personalizado. Para ello, es fundamental considerar cinco procesos clave: inflamación, pérdida de la homeostasis de la superficie ocular, inestabilidad de la película lagrimal, hiperosmolaridad y alteraciones neurosensoriales. (3)
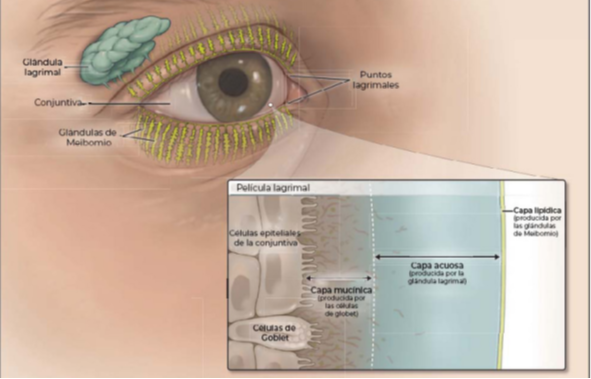
Foto tomada de httpssci hubse
De acuerdo con la última reunión del TFOS (DEWS III) en octubre de 2024, el abordaje terapéutico del ojo seco se está tornando más complejo al comprender en profundidad los eventos biológicos que ocurren en la unidad funcional lagrimal (UFL). A partir de la comprensión de estos mecanismos fisiopatológicos, han surgido recientemente estrategias innovadoras de manejo, entre las que destaca la aplicación de nanotecnología. (5)
La incorporación de la inteligencia artificial y la nanotecnología, que permite la manipulación y fabricación de materiales y dispositivos a escala nanométrica, ha aportado ventajas en diversas disciplinas, tales como a física, química, biología, ingeniería y ciencias sociales. (6) En el ámbito de la salud, la nanotecnología ha facilitado el desarrollo de nuevos tratamientos y medicamentos, incluyendo sistemas de liberación controlada de fármacos y avances en diagnóstico y tratamiento. En el caso del ojo seco, algunos tratamientos convencionales, como los antiinflamatorios, lubricantes e inmunomoduladores a partir de colirios oftálmicos, pueden ocasionar efectos adversos en la superficie ocular, lo que ha impulsado la búsqueda de nuevos sistemas de liberación de fármacos.
Nanofarmacología: una apuesta para el tratamiento del ojo seco
La nanotecnología emerge como una solución innovadora para el tratamiento del síndrome del ojo seco, una afección que afecta a millones de personas en todo el mundo. Esta enfermedad se caracteriza por la pérdida de la película lagrimal y puede provocar síntomas como ardor, irritación y dolor ocular.
Uno de los principales inconvenientes del tratamiento convencional mediante la administración tópica oftálmica, es la baja biodisponibilidad de los fármacos, los cuales deben atravesar barreras físicas y anatómicas en el segmento anterior del ojo, además de generar efectos adversos bien sea por su principio activo y/o excipientes. (7) En este contexto, las nanopartículas podrían mejorar el proceso de absorción de fármacos y, a su vez, reducir los efectos adversos asociados a medicamentos como la ciclosporina, lubricantes y antiinflamatorios, que a menudo afectan la superficie ocular.
Un ejemplo de los nuevos sistemas de liberación de fármacos son los liposomas, vesículas esféricas formadas por una o más bicapas lipídicas que encapsulan fármacos. Los liposomas se han convertido en una herramienta valiosa en la nanomedicina, ya que ofrecen ventajas como la liberación controlada, mejoran la biodisponibilidad al atravesar con mayor facilidad las barreras dinámicas y estáticas de la superficie ocular, y pueden diseñarse para dirigirse a tejidos específicos mediante modificaciones en su composición lipídica o la conjugación con ligandos específicos. (5)(8) Esto incrementa la concentración del fármaco en el sitio deseado y minimiza los efectos secundarios.
Avances en terapias con nanopartículas
- Desarrollo de soluciones oftálmicas: diversas investigaciones han explorado estrategias para optimizar la biodisponibilidad de los medicamentos oftálmicos. En contexto, se han diseñado soluciones oftálmicas que utilizan nanopartículas capaces de proporcionar efectos hidratantes prolongados. Estos tratamientos no solo buscan aliviar los síntomas, sino también ofrecer propiedades antiinflamatorias y antimicrobianas, superando las limitaciones de las lágrimas artificiales tradicionales. Actualmente, se investigan aplicaciones clínicas de nanogotas y lágrimas artificiales inteligentes, cuyas nuevas formulaciones incorporan liposomas y nanomicelas para restaurar las tres capas de la película lagrimal y mejorar así las condiciones farmacocinéticas. (6)(9)
2. Terapia génica: un enfoque innovador en desarrollo es el uso de nanopartículas como vehículo para transportar un plásmido que codifica la proteína MUC5AC, esencial para mantener la homeostasis del fluido lacrimal. En estudios con modelos animales, este tratamiento ha demostrado ser eficaz en la restauración de la producción normal de lágrimas y en la mejora de la protección ocular. (10)
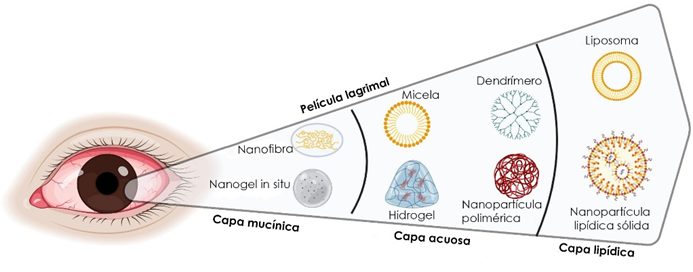
Ventajas del uso de nanopartículas en el tratamiento del ojo seco
- Liberación sostenida: las nanopartículas permiten una liberación controlada y sostenida de los fármacos, lo que mejora su biodisponibilidad y eficacia. Esto significa que una mayor proporción del medicamento alcanza las diferentes estructuras oculares, superando la limitación de las lágrimas artificiales convencionales, donde menos del 5 % alcanzan su objetivo. (12)
- Propiedades adicionales: además de su función hidratante, las nanopartículas pueden poseer propiedades antiinflamatorias, antibacterianas y antimicrobianas, contribuyendo así a mejorar la salud ocular general y a reducir el riesgo de infecciones. (13)
- Biocompatibilidad y seguridad: las nanopartículas desarrolladas son estériles, biodegradables y producidas mediante métodos sostenibles. Esto minimiza el riesgo de efectos secundarios adversos, una preocupación común con los tratamientos tradicionales.
Desafíos y perspectivas
A pesar de los avances en la nanofarmacología aplicada al tratamiento del ojo seco, aún persisten varios desafíos. Uno de los principales es la estabilidad de las formulaciones, ya que mantener su integridad tanto durante el almacenamiento como en su uso sigue siendo un reto significativo.
Por otro lado, la regulación y aprobación de estos tratamientos exige cumplir con estrictas normativas, lo que requiere pruebas exhaustivas de seguridad y eficacia, un proceso que puede resultar largo y costoso. Finalmente, los costos de desarrollo representan otro desafío importante, ya que la investigación y el desarrollo de nuevas formulaciones basadas en nanopartículas requieren inversiones sustanciales.
Referencias
- O’Neil EC, Henderson M, Massaro-Giordano M, Bunya VY. Advances in dry eye disease treatment. Curr Opin Ophthalmol [Internet]. 2019 May;30(3):166–78. Available from: https://pubmed.ncbi.nlm.nih.gov/30883442
- Alves M, Asbell P, Dogru M, Giannaccare G, Grau A, Gregory D, et al. TFOS Lifestyle Report: Impact of environmental conditions on the ocular surface. Ocul Surf [Internet]. 2023;29:1–52. Available from: https://www.sciencedirect.com/science/article/pii/S1542012423000332
- Bron AJ, de Paiva CS, Chauhan SK, Bonini S, Gabison EE, Jain S, et al. TFOS DEWS II pathophysiology report. Ocul Surf [Internet]. 2017;15(3):438–510. Available from: http://www.sciencedirect.com/science/article/pii/S1542012417301349
- Clayton JA. Dry Eye. N Engl J Med. 2018 Jun;378(23):2212–23.
- Wang T-Z, Liu X-X, Wang S-Y, Liu Y, Pan X-Y, Wang J-J, et al. Engineering Advanced Drug Delivery Systems for Dry Eye: A Review. Bioeng (Basel, Switzerland). 2022 Dec;10(1).
- Lv Z, Li S, Zeng G, Yao K, Han H. Recent progress of nanomedicine in managing dry eye disease. Adv Ophthalmol Pract Res. 2024;4(1):23–31.
- Agrahari V, Mandal A, Agrahari V, Trinh HM, Joseph M, Ray A, et al. A comprehensive insight on ocular pharmacokinetics. Drug Deliv Transl Res. 2016 Dec;6(6):735–54.
- Coco G, Buffon G, Taloni A, Giannaccare G. Recent Advances in Nanotechnology for the Treatment of Dry Eye Disease. Nanomater (Basel, Switzerland). 2024 Apr;14(8).
- Huang Y, Wang L, Jin H. cRGD-Conjugated Bilirubin Nanoparticles Alleviate Dry Eye Disease Via Activating the PINK1-Mediated Mitophagy. Invest Ophthalmol Vis Sci. 2024 Nov;65(13):55.
- Contreras-Ruiz L, Zorzi GK, Hileeto D, López-García A, Calonge M, Seijo B, et al. A nanomedicine to treat ocular surface inflammation: performance on an experimental dry eye murine model. Gene Ther. 2013 May;20(5):467–77.
- Philip AK. Nanotechnology-based Therapeutic Strategies for Dry Eye Disease . J Explor Res Pharmacol [Internet]. 8(3):253–62. Available from: https://www.xiahepublishing.com/2572-5505/JERP-2023-00034
- Joseph M, Trinh HM, Cholkar K, Pal D, Mitra AK. Recent perspectives on the delivery of biologics to back of the eye. Expert Opin Drug Deliv. 2017 May;14(5):631–45.
13. Kim TY, Lee G-H, Mun J, Cheong S, Choi I, Kim H, et al. Smart contact lens systems for ocular drug delivery and therapy. Adv Drug Deliv Rev. 2023 May;196:114817.

Sandra Carolina Durán Cristiano, O.D
Estudiante Doctorado Universidad Complutense de Madrid.
Docente de la Facultad de Medicina del programa de Optometría de la Universidad CES
Editora del Área de Superficie Ocular





