La queratoconjuntivitis vernal (QCV) es una enfermedad crónica que afecta la superficie ocular, ya que compromete la conjuntiva y la córnea y presenta episodios remitentes en el proceso de inflamación. Se ha establecido que la mayor frecuencia de esta patología se da en pacientes que viven en regiones cálidas y secas, en este caso generando la atención en Centroamérica y Suramérica. La edad de aparición suele ser en la primera década de vida, especialmente entre los 6 y 7 años, con tendencia a desaparecer en la pubertad. De aquí se desprenden teorías etiológicas de origen hormonal, donde es preciso destacar que se manifiesta más en hombres que en mujeres. (1)
En la presentación clínica de la QCV, se identifican tres fenotipos que son principalmente: tarsal, limbar y mixto. Las papilas en el tarso, en el limbo (nódulos de Horner-Trantas), o en ambos, serán la clave de esta clasificación. La sintomatología de esta entidad se puede superponer a la de la conjuntivitis alérgica; sin embargo, la existencia de una fotofobia intensa, acompañada de dolor, puede ser característica de la QCV. En casos severos, se pueden manifestar signos como: úlceras en escudo, vascularización corneal, retardo en la reepitelización y disminución de la agudeza visual. Dentro de las opciones de tratamiento, existe una gran variedad de medicamentos entre los que se encuentran los antihistamínicos tópicos y sistémicos, los estabilizadores de la membrana de los mastocitos, también de forma tópica y sistémica, AINES, corticosteroides e inmunomoduladores también están en la lista de opciones, dependiendo de la severidad de la presentación clínica y la respuesta o resistencia al tratamiento. (1-3)
Justo en esa fase, en la cual las manifestaciones son severas, el tratamiento es negativo y los efectos secundarios de medicamentos como los corticoides, o la toxicidad de la administración crónica, disminuyen la calidad de vida del afectado y generan la necesidad de buscar otras alternativas para el manejo de estos pacientes. Por tal motivo, surgen estrategias como el uso de omalizumab. Este medicamento, se trata de un anticuerpo monoclonal humanizado recombinante, que reduce los niveles de IgE circulante, al unirse a su dominio C3e, también reduce la expresión de genes para los receptores de alta afinidad para la IgE a nivel de los mastocitos y los basófilos. (2,4)
Omalizumab se ha indicado para prevenir exacerbaciones severas y evitar el uso de corticoides sistémicos. Este fármaco está aprobado para uso en pacientes mayores de 12 años y se usa sistémicamente en el caso de asma grave y urticaria intensa crónica. Es importante destacar que la aplicación del medicamento es subcutánea, y tiene una vida media de 26 días, lo que hace que su administración sea cada 2 o 4 semanas y la dosis dependerá del peso del paciente, oscilando entre 150 a 375 mg. También dependerá de la cantidad de IgE en suero. (2,4)
Por lo anterior, se ha contemplado su uso a nivel ocular, como en el caso de QCV. En este sentido, Manti et al., 2021, publican un reporte de casos que han sido manejados con omalizumab. Básicamente se trata de casos severos en donde la sintomatología del paciente es marcada, afectando su calidad de vida y hay resistencia con diferentes medicamentos como estabilizadores de membrana, corticoides, antihistamínicos, e incluso ciclosporina A. Los resultados del tratamiento por tres meses con Omalizumab, mostraron mejoría significativa de los signos clínicos, donde las papilas casi desaparecen y, adicionalmente, los pacientes mostraron un sustancial alivio de los síntomas. Además de los resultados positivos del tratamiento, los autores indican que este es un paso importante para estructurar ensayos clínicos aleatorizados con un tiempo de evolución largo, para lograr una aprobación definitiva del uso de omalizumab en el tratamiento de QCV resistente. (5)
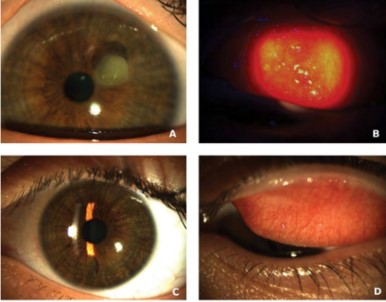
Lo mismo sucede con Mozo Cuadrado et al., 2020, quienes reportan un caso de QCV en un paciente de 14 años que presentó tratamiento fallido con olopatadina, dexametasona y ciclosporina. Al paciente se le administró omalizumab sistémico subcutáneo cada 15 días y según la evolución, se disminuyó a frecuencia mensual. Uno de los factores preponderantes para iniciar el tratamiento con este medicamento, fueron los resultados elevados de IgE en sangre. Los hallazgos cínicos más graves eran las papilas de gran tamaño, nódulos de Horner-Trantas y úlcera en escudo, los cuales se resolvieron satisfactoriamente. (2) Ver figura 1.
La QCV es una enfermedad cuyo proceso fisiopatogénico aún no está completamente comprendido; lo que se sabe, es que la respuesta inflamatoria, mediante una liberación de citoquinas específicas que se están estudiando en la actualidad como biomarcadores. La respuesta positiva frente a omalizumab, sugiere que, entre esa respuesta inmune, se encuentra una importante mediación de IgE, pero hasta se han descrito mecanismos autoinmunes para explicar la patología. La evidencia requiere fortalecerse para promover la aplicación de omalizumab en pacientes con QCV resistente.
REFERENCIAS
- Brindisi G, Cinicola B, Anania C, De Castro G, Nebbioso M, Del Giudice MM, et al. Vernal keratoconjunctivitis: state of art and update on treatment. Acta Biomed. 2021;92:1–7.
- Mozo Cuadrado M, Orive Bañuelos A, Etxebarria Ecenarro J. Vernal keratoconjunctivitis (VKC) successfully treated with omalizumab. J Fr Ophtalmol. 2020;43(6):e193–5.
- Mehta JS, Chen WL, Cheng ACK, Cung LX, Dualan IJ, Kekunnaya R, et al. Diagnosis, Management, and Treatment of Vernal Keratoconjunctivitis in Asia: Recommendations From the Management of Vernal Keratoconjunctivitis in Asia Expert Working Group. Front Med. 2022;9(August).
- Kırıkkaya E, Değirmenci P. Effects of omalizumab on allergic conjunctivitis. Int Ophthalmol. 2022;42(1):167–75.
- Manti S, Parisi GF, Papale M, Marseglia GL, Licari A, Leonardi S. Clinical efficacy and safety of omalizumab in conventional treatment-resistant vernal keratoconjunctivitis: Our experience and literature review. Immunity, Inflamm Dis. 2021;9(1):3–7.





