Una de las sensaciones más desagradables que los humanos experimentan es el miedo al dolor. Según la duración, puede ser agudo o crónico, cuando dura más de tres meses. En otro aspecto, se puede clasificar en nociceptivo cuando es producido por estímulos nocivos, o neuropático, que se genera por un mal funcionamiento del sistema nervioso. Es importante conocer que las neuronas nociceptivas localizadas en la raíz del ganglio dorsal son las encargadas del dolor agudo y el dolor es directamente proporcional a la intensidad del estímulo. Adicionalmente, cuando este desaparece, el dolor también. Por otro lado, el dolor neuropático se caracteriza por una intensidad fuera de proporción y se genera incluso sin la presencia de un estímulo dañino. Es más, los pacientes pueden experimentar dolor con estímulos que usualmente serían benignos (alodinia) o presentarse como respuesta exageradamente dolorosa ante un estímulo (hiperalgesia).1
Cuando hay dolor crónico, puede existir anormalidad de la plasticidad en las conexiones sinápticas del sistema nervioso central (SNC), lo que conlleva a la hiperalgesia o alodinia, alterando de esta manera la modulación descendente de la respuesta dolorosa. Esta sería la representación clásica del dolor neuropático. Siendo así, se ha afirmado que este tipo de dolor tiene un componente genético importante, que podría afectar la neurotransmisión, la respuesta inmune y el metabolismo. También se ha llegado a afirmar que variaciones en la catecol-O-metiltransferasa (COMT), pueden causar cierta susceptibilidad al dolor.1
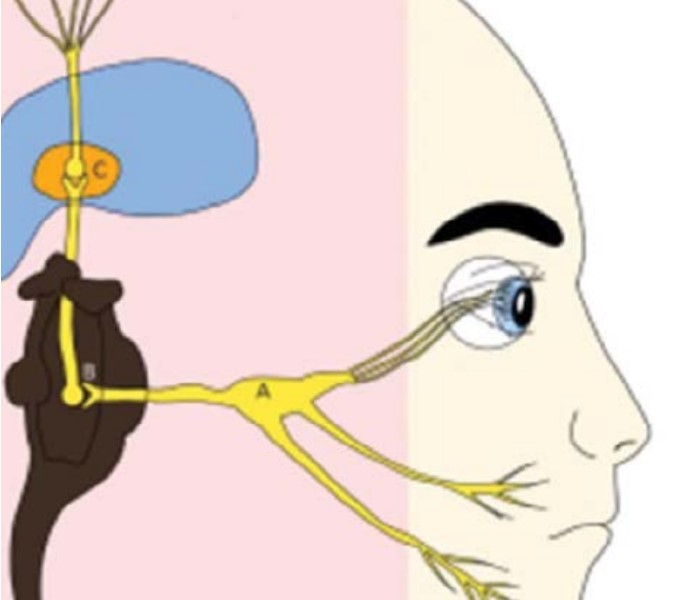
En el caso de la superficie ocular, el inconfort, que sería el mismo dolor neuropático, puede ser producto de factores como el estrés, la depresión, la ansiedad y hasta factores socioculturales o la presencia de dolor crónico en otras partes del cuerpo. El origen de este dolor es complejo, donde tanto el SNC como el periférico tomarían parte. Si se analiza el dolor corneal, se puede identificar que puede ser neurotrófico, como el caso de la queratitis herpética o nociceptivo como el caso de la cirugía. En todo caso, la hiperosmolaridad es una clara protagonista, ya que es el punto de partida de la inflamación de la superficie ocular, que estimula las terminales nerviosas de la córnea a nivel epitelial, que posteriormente estimula la liberación de neuropéptidos de los nervios corneales. Todo lo anterior, genera sintomatología neuropática como la hiperalgesia o la sensación de quemazón. Prueba de lo anterior, es que la microscopía confocal de pacientes con ojo seco severo ha mostrado cambios en el plexo nervioso subbasal, así como baja densidad, engrosamiento, crecimiento y tortuosidad de las terminales nerviosas. Esto sería explicado por disfunciones somatosensoriales que afectan el SNC y se relacionarían directamente con el dolor neuropático.1 Ver figura 1.
Ya que el dolor neuropático de la superficie ocular se origina desde mecanismos complejos, el tratamiento puede abarcar diferentes espectros de acción entre los cuales se destacan:
- Tratamiento tópico para aliviar el dolor. En este grupo se encuentran los lubricantes oculares, los antiinflamatorios e inmunomoduladores, la terapia neuroregenerativa y los lentes de contacto terapéuticos.
- Terapia oral para el manejo de la sensibilidad central o periférica. A este grupo pertenecen los gabapentinoides, los inhibidores de la recaptación de serotonina y norepinefrina y los antidepresivos tricíclicos.
- Terapia invasiva complementaria. Aquí se encuentran medicamentos como la toxina botulínica periocular, los bloqueadores nerviosos perioculares, y el bloqueo de ganglios.
- Terapia no farmacológica.Como la terapia cognitiva comportamental.1
De la variedad de grupos farmacológicos mencionados anteriormente, la gabapentina ha sido objeto de investigación fuerte en los últimos años. Ongun et al., 2019, realizaron una investigación comparando dos grupos diagnosticados con ojo seco severo con dolor neuropático. Un grupo se trató con ciclosporina A y lubricante ocular y el otro con ciclosporina A, lubricante y gabapentina. Los resultados muestran que el grupo que incluye la gabapentina mostró diferencias significativas positivas en términos de mejoría de la estabilidad lagrimal y manejo del dolor neuropático.2
Michael et al., 2020, reportaron un caso de dolor ocular neuropático con ocho meses de evolución, con un antecedente de LASIK que se complicó a ectasia. Posterior al tratamiento oral con gabapentina de 300 mg dos veces al día, por 3 semanas, el dolor del paciente desapareció completamente.3
Es importante que complementario al examen riguroso para detectar alteraciones en la superficie ocular, también que se evalúe más a fondo la presencia de dolor neuropático, para establecer mecanismos alternativos de tratamiento conducentes al alivio completo del dolor crónico.
REFERENCIAS
- Ebrahimiadib N, Yousefshahi F, Abdi P, Ghahari M, Modjtahedi BS. Ocular neuropathic pain: An overview focusing on ocular surface pains. Clin Ophthalmol. 2020; 14:2843–54.
- Ongun N, Ongun GT. Is gabapentin effective in dry eye disease and neuropathic ocular pain? Acta Neurol Belg [Internet]. 2021;121(2):397–401. Available from: https://doi.org/10.1007/s13760-019-01156-w
- Michael R, Jeffers J V., Messenger W, Aref AA. Gabapentin for presumed neuropathic ocular pain. Am J Ophthalmol Case Reports [Internet]. 2020;19:100836. Available from: https://doi.org/10.1016/j.ajoc.2020.100836






