La miopía axial es motivo de creciente preocupación a nivel mundial, ya que se estima que para el año 2050 casi la mitad de la población presentará este estado refractivo. Esto tendrá consecuencias significativas, como la disminución de la visión y alteraciones en el polo posterior que podrían ser discapacitantes e irreversibles. Por este motivo, se han desarrollado diferentes estrategias para reducir la progresión de la miopía, que abarcan desde cambios comportamentales hasta el uso de medicamentos, lentes oftálmicos y lentes de contacto (LC) con diseños especiales. (1)
Entre estas estrategias, destaca el uso de atropina, que ha sido evaluada en diferentes concentraciones. Las dosis bajas, como 0.01 % y 0.025 %, se utilizan en protocolos que aprovechan su función como medicamento antimuscarínico. Otra propuesta relevante es el empleo de LC blandos diseñados específicamente para controlar la focalización de la luz tanto en el centro como en la periferia de la retina, evitando desenfoques luminosos que favorezcan el crecimiento axial. (2)–(4)
Con base en lo anterior, ha surgido la necesidad de investigar métodos que permitan a los LC liberar atropina de manera controlada. Este enfoque, al actuar como un reservorio de medicamento, podría mejorar tanto la eficacia como la adherencia al tratamiento. Aunque la atropina en gotas ha demostrado ser eficaz, presenta limitaciones como una biodisponibilidad reducida, que puede ser inferior al 5 %, y su rápida eliminación a través del sistema de drenaje lagrimal. Por el contrario, los LC podrían aumentar la biodisponibilidad hasta en un 50 % mediante una liberación sostenida, lo que incrementaría la efectividad del fármaco y reduciría los efectos secundarios. (5)
Con esta premisa, Aziz y colaboradores (2024) realizan un estudio con el objetivo de evaluar la viabilidad de unir atropina a LC de etafilcón A mediante una reacción de esterificación. Este estudio inicial representa un avance hacia la propuesta un tratamiento combinado que incorpore el diseño del LC para manejar la miopía junto con la liberación sostenida de atropina a través de este. Esto sería posible mediante la unión covalente de la atropina al material del lente de contacto. (6)
Para alcanzar el objetivo, los autores utilizaron etafilcón A como sustrato para la unión del medicamento. Los lentes se sometieron a un proceso de activación mediante el tratamiento con una mezcla de 1-etil-3-(3-dimetilaminopropil) carbodiimida (EDC) y N-hidroxisuccinimida (NHS). Este proceso de activación permitió crear sitios reactivos en la superficie de los lentes, facilitando la formación de enlaces covalentes con los grupos hidroxilo de la atropina. (6)
Posteriormente, los LC fueron sumergidos en una solución preparada de atropina, controlando cuidadosamente el tiempo de inmersión y la concentración, para asegurar la unión adecuada del medicamento al material del lente. Tras la inmersión, los lentes se lavaron para eliminar cualquier atropina no unida al material. La cantidad de atropina adherida al LC fue cuantificada mediante cromatografía líquida de alta eficiencia (HPLC, por su sigla en inglés), evaluando así la efectividad de la unión covalente. Finalmente, el perfil de liberación de atropina se analizó incubando los lentes en un medio de liberación y midiendo la cantidad de atropina liberada en función del tiempo.6 Ver Figura 1.
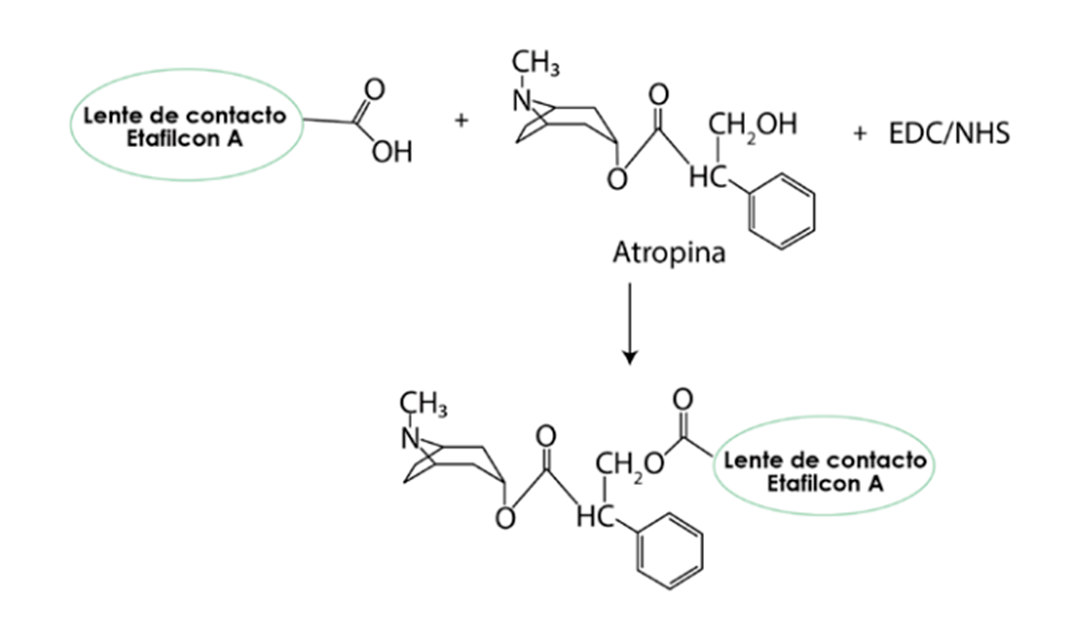
Figura 1. Ilustración del proceso de esterificación de la atropina al material del lente de contacto. (6)
Al analizar los resultado, los autores determinaron que, aunque el material etafilcón A contiene grupos de ácidos carboxílicos que podrían facilitar la formación de enlaces éster, no se logró con éxito la unión química necesaria para una liberación efectiva del medicamento. Este hallazgo destaca ciertos desafíos que condicionan la unión covalente de la atropina al LC. (6)
Entre los principales desafíos identificados se encuentra la naturaleza hidrofóbica de la atropina, en contraste con las propiedades hidrofílicas del etafilcón, lo que dificulta la formación de enlaces covalentes. Además, la estructura no plana de la atropina representa un obstáculo, ya que impide su unión eficiente a los grupos aniónicos presentes en el etafilcón A, esenciales para el proceso de esterificación. Otro factor crítico es la presencia de agua como solvente prótico, que puede reducir la nucleofilicidad de los aniones hidroxilo, también indispensables para la esterificación. Estas condiciones limitan la reacción entre la atropina y los grupos de ácidos carboxílicos del etafilcón. (6)
Otro aspecto analizado por los autores es que, a pesar de usar EDC y NHS como agentes de entrecruzamiento para facilitar la esterificación, las condiciones no fueron suficientes para lograr una unión covalente exitosa entre la atropina y el lente. Estos desafíos destacan la necesidad de seguir investigando, dada la complejidad de la situación. (6)
Sin embargo, el estudio presenta un panorama prometedor: la implementación de LC como sistemas de administración de fármacos para el manejo de la miopía surge como una alternativa prometedora para optimizar la eficacia terapéutica. Este enfoque requiere una inversión significativa de recursos para superar los desafíos mencionados, incluyendo la exploración de otros materiales. En este sentido, los esfuerzos investigativos se enfocarán en identificar las técnicas adecuadas para lograr una unión química efectiva entre la atropina y el material del lente. (6)
Referencias
- Holden BA, Fricke TR, Wilson DA, Jong M, Naidoo KS, Sankaridurg P, et al. Global Prevalence of Myopia and High Myopia and Temporal Trends from 2000 through 2050. Ophthalmology. el 1 de mayo de 2016;123(5):1036–42.
- Yam JC, Jiang Y, Tang SM, Law AKP, Chan JJ, Wong E, et al. Low-Concentration Atropine for Myopia Progression (LAMP) Study: A Randomized, Double-Blinded, PlaceboControlled Trial of 0.05%, 0.025%, and 0.01% Atropine Eye Drops in Myopia Control. Ophthalmology. el 1 de enero de 2019;126(1):113–24.
- Chamberlain P, Peixoto-De-Matos SC, Logan NS, Ngo C, Jones D, Young G. A 3-year Randomized Clinical Trial of MiSight Lenses for Myopia Control. Optometry and Vision Science. el 1 de agosto de 2019;96(8):556–67.
- Chamberlain P, Lazon de la Jara P, Arumugam B, Bullimore MA. Axial length targets for myopia control. Ophthalmic and Physiological Optics. el 1 de mayo de 2021;41(3):523–31.
- Irimia T, Ghica MV, Popa L, Anuţa V, Arsene AL, Dinu-Pîrvu CE. Strategies for improving ocular drug bioavailability and cornealwound healing with chitosan-based delivery systems. Vol. 10, Polymers. MDPI AG; 2018.
- Abdullah Aziz M, Kuppusamy R, Mazumder K, Hui A, Maulvi F, Stapleton F, et al. Absorption and attachment of atropine to etafilcon A contact lenses. Contact Lens and Anterior Eye. el 1 de octubre de 2024;47(5).

Martín Edisson Giraldo Mendivelso. Optómetra ULS, Magister Ciencias de la Visión. ULS. Especialista en Segmento Anterior y Lentes de Contacto USTA, FELLOW IACLE. Profesor Universidad CES, Medellín. [email protected].






